InnomarLive Sommaire: Commercialisation au Canada
By Innomar Strategies
Le 28 novembre 2019, InnomarConsultingMC a accueilli sa 10e conférence InnomarLive intitulée« Commercialisation au Canada : Synergies entre les organismes de réglementation et les agences d’évaluation des technologies de la santé ». Présidée par Durhane Wong-Reiger, président et premier dirigeant de la Canadian Organization for Rare Disorders (CORD), cette conférence d’une journée comprenait des présentations et des débats d’experts réunissant d’importants leaders d’opinion canadiens sur des sujets aussi divers que la réglementation, les organismes d’évaluation des technologies de la santé, les payeurs privés, l’industrie et la défense des patients. Au cours de la journée, les participants ont eu un aperçu des efforts transparents et collaboratifs consentis pour accélérer l’accès aux produits thérapeutiques, de l’importance d’un accès en temps opportun aux médicaments novateurs pour les patients grâce à des outils comme les données concrètes et les principales étapes de la commercialisation des produits.
Santé Canada et les organismes d’ÉTS ont consenti beaucoup d’efforts pour accélérer le processus complexe permettant aux Canadiens d’avoir accès à de nouveaux médicaments spécialisés.
Megan Bettle, directrice, Centre d’excellence réglementaire, statistiques et essais cliniques de la Direction des produits biologiques et des thérapies génétiques à Santé Canada, a présenté un plan pour un « système réglementaire agile qui favorise un meilleur accès aux produits thérapeutiques en fonction des besoins du système de santé ». Le plan prévoit : une collaboration élargie avec les partenaires de la santé, y compris l’Agence canadienne des médicaments et des technologies de la santé (ACMTS), par l’harmonisation des évaluations des technologies de la santé, appelée « R2D2 » et la mise en œuvre d’un mécanisme pour la prestation de conseils scientifiques parallèles précoces, un accès plus opportun aux médicaments et aux dispositifs et une utilisation accrue des données concrètes.
Le fait de déposer la demande tôt dans le processus réduira considérablement le délai entre l’approbation de Santé Canada et les recommandations des organismes d’ÉTS.
Trevor Richter, directeur des Évaluations de médicaments pour l’Agence canadienne des médicaments et des technologies de la santé (ACMTS), a parlé du processus d’évaluation harmonisé et de ses deux éléments :le fait de remplir le préavis de conformité et le consentement du fabricant au partage de renseignements entre Santé Canada et les organismes d’évaluation des technologies de la santé. Même si ce processus n’est pas obligatoire, le dépôt précoce des avis de conformité réduira la période de latence entre l’approbation par Santé Canada de la mise en marché et les recommandations des organismes d’ÉTS, ce qui rendra les produits plus rapidement accessibles pour les patients.
Sylvie Bouchard, directrice, Institut national d’excellence en santé et en services sociaux (INESSS), et Sang Mi Lee, gestionnaire principale, Alliance pancanadienne pharmaceutique, ont parlé des objectifs de leurs organismes respectifs et de leurs efforts en matière de commercialisation. Sylvie a présenté plusieurs cibles de la Stratégie québécoise des sciences de la vie, dont la synchronisation des recommandations d'inscription de l’INESS et de l’ACMTS pour que l’écart moyen entre les deux soit d’un mois maximum, et la réduction du délai entre la délivrance de l’avis de conformité et le remboursement par le gouvernement du Québec. Elle a également décrit le nouveau cadre d’évaluation de l’INESS, y compris une approche d’évaluation fondée sur des critères, la saisie des données fondées sur l’expérience des patients et le concept des avantages potentiels dans certaines situations exceptionnelles.
Anne Tomalin, vice-présidente, Qualité, Réglementation et Innocuité chez Innomar Strategies, a présenté les questions réglementaires qui doivent être prises en compte lors de la commercialisation d’un produit au Canada. Anne a présenté de nombreux sujets à l’auditoire, y compris les Certificats de protection supplémentaire, la nouvelle structure des droits pour les présentations de drogues, l’accès aux médicaments génériques, l’utilisation de données concrètes, la transparence des soumissions et des appels, la déclaration obligatoire des RIM par les hôpitaux et les mises à jour du Programme d’accès spécial de Santé Canada.
Les organismes de réglementation canadiens, les organisations d’ÉTS et les payeurs reconnaissent la valeur des données concrètes pour évaluer la qualité générale et le caractère approprié des soins de santé.
L’importance des données concrètes et l’intérêt croissant pour celles-ci a été un sujet récurrent pendant toute la journée. Don Husereau, chercheur principal du Institute of Health Economics, a parlé de l’utilisation des données concrètes dans les stratégies de commercialisation. Don a également mentionné comment les organismes de réglementation canadiens, les organismes d’évaluation des technologies de la santé et les payeurs considèrent et apprécient les données concrètes, citant une publication récente : « les dirigeants des systèmes de santé et les payeurs en apprécient la valeur réelle dans l’évaluation de la qualité et du caractère approprié des soins de santé, qui peuvent inclure ou non des médicaments ».1
Il est important de consulter rapidement les payeurs privés afin de permettre aux fabricants d’obtenir des conseils sur la présentation et pour permettre aux payeurs privé d’effectuer des tâches en parallèle.
Lors du débat d’experts réunissant des payeurs privés, Bobby Currie, directrice de la stratégie en matière de médicaments de la Great-West, Daria O’Reilly, économiste principale en santé, experte-conseil en pharmacie, Telus et Ned Pojskic, chef, Relations avec les pharmacies et les prestataires de soins, Green Shield Canada, ont discuté de la commercialisation dans un environnement en transformation et de la façon d’optimiser les échanges avec les payeurs privés pendant le processus menant à l’accès au marché. Tous les experts ont mentionné l’importance de consulter rapidement les payeurs privés afin de permettre aux fabricants d’obtenir des conseils sur la présentation et pour permettre aux payeurs privé d’effectuer le plus de tâches parallèles possibles et de comprendre plus rapidement les filières du fabricant. Ils ont également mentionné la nécessité d’adapter les modèles et de recueillir les renseignements que les payeurs privés veulent connaître, sur la productivité et les handicaps en particulier.
Pamela Fralick, présidente, Médicaments novateurs Canada (MNC), a parlé des possibilités qui s'offrent à l'industrie des médicaments novateurs du Canada et des défis qu’elle aura à relever. Elle a parlé de défendre les solutions visant à atténuer l’incidence de la réforme du Conseil d’examen des prix des médicaments brevetés (CEPMB) en raison de laquelle certaines compagnies ont déjà décidé de retarder les investissements, les lancements et les embauches et de mettre fin à des essais cliniques. Elle a également mentionné les possibilités associées au régime national d’assurance-médicaments, à l’accès aux médicaments pour les maladies rares et au groupe de travail de l’industrie dont le but est d’élaborer des options politiques.
Obtenez un PDF e ce sommaire.
D’autres représentants de l’industrie, le cadre Eric Tse et Frédéric Lavoie, vice-président Accès et Relations avec le gouvernement du Canada, Pfizer Canada, ont parlé de l’incertitude qui règne dans l’environnement en transformation, de ce que cela signifie en matière d’innovation et de capacité à rendre les médicaments disponibles pour les patients ainsi que des facteurs à prendre en compte pour tracer la voir de la commercialisation au Canada.
Un élément important concernant la commercialisation est la planification de la stratégie et de la logistique de distribution du produit. Dan Chiasson, président et chef de la direction de l'Association canadienne de la gestion de l'approvisionnement pharmaceutique (ACGAP), a présenté un portait détaillé de l'environnement d’approvisionnement canadien ainsi que des recommandations et des facteurs à prendre en compte pour la réussite du lancement des produits comme la circulation des produits, les fonds et les données.
Siofradh McMahon, gestionnaire principale, Applications cliniques et Affaires réglementaires, Centre for Commercialization of Regenerative Medicine (CCRM), a présenté à l’auditoire un aperçu des différences et des défis associés à la commercialisation de traitements vivants. Appelée Produits thérapeutiques avancés, une nouvelle voie a été approuvée en 2019 pour faciliter le développement d’une stratégie réglementaires pour ces thérapies cellulaires et génétiques. Siofradh a mentionné que l’avenir des thérapies vivantes était prometteur au Canada et qu’il y a environ 95 essais cliniques sur des thérapies cellulaires et génétiques en cours au Canada.
Le point de vue du patient est un facteur important du parcours de commercialisation.
Ian Steadman, un défenseur des patients et membres du conseil d’administration de la CORD, et Durhane Wong-Reiger ont parlé éloquemment de l’incidence et de l’importance du point de vue du patient dans le parcours de commercialisation et de la nécessité d’offrir un accès opportun aux nouvelles thérapies. Ian a parlé de son parcours personnel en tant que patient atteint d’un trouble génétique rare, le syndrome de Muckle-Wells, des épreuves qu’il a dû surmonter et l’impact que les traitements ont sur sa vie. Grâce à un nouveau traitement efficace, sa fille, qui souffre également du syndrome de Muckle-Wells, ne connaîtra pas les mêmes problèmes et épreuves que son père.
Abordant le parcours de commercialisation de façon holistique, Sandra Anderson d’Innomar Strategies a résumé les points de vue, les exigences de planification proactive et les facteurs dont les fabricants doivent tenir compte pour le lancement de leurs produits. Elle a également présenté les principales phases et les principaux plans à établir (figure 1) lors de chacune des étapes en mettant l’accès sur les facteurs clés pour une commercialisation réussie au Canada.
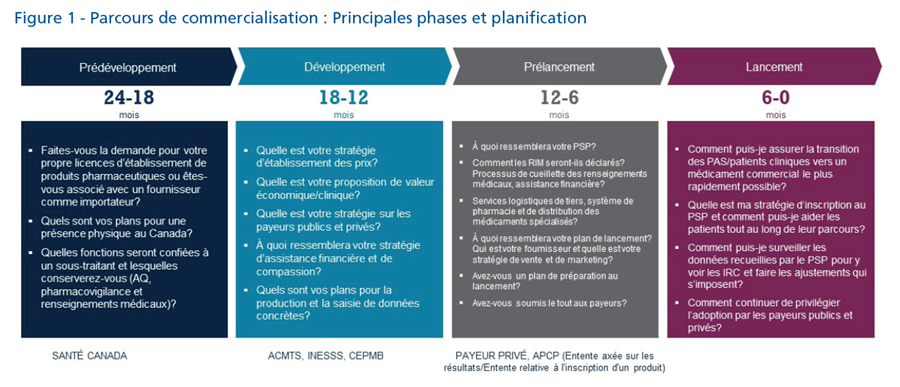
Le rôle de la commercialisation est crucial pour la réussite du lancement d’un nouveau produit thérapeutique. Il y a toutefois de nombreux éléments dont il faut tenir compte, comme une planification précoce, la mobilisation des intervenants, des cliniciens et des patients, qui permettent d’optimiser le parcours, l’évitement des retards dans la génération de revenus et l’accès rapide aux médicaments par les patients.
